作为中国迅速发展的生物制药行业的领导公司,三生制药拥有30余种上市产品,30余种在研产品,其中22种国家一类新药,主要涵盖肿瘤科、自身免疫性疾病、肾科、代谢、皮肤科以及其他相关治疗领域。三生制药具有生物药和化药两个领域的研究平台,涵盖从基础研发、临床前研究、临床试验到新药注册上市的药物开发全过程。
为了更好支撑临床试验的项目的顺利开展,2018年三生制药与百奥知签订了临床试验信息化平台采购协议,全方位引进百奥知临床研究信息化解决方案,涵盖如下软件系统。
1
数据管理解决方案(EDC、RTSM、MedCoding)
2
项目管理解决方案(CTMS)
3
文档管理解决方案(eTMF)
4
药物警戒解决方案(PV)
以上系统已经陆续上线,服务于三生制药多个临床试验项目。
近期百奥知eTMF与CTMS系统进行了迭代升级,应三生制药邀请,百奥知为三生制药及外包CRO临床运营团队进行了为期3天的新版本系统操作培训。
2019年6月17日,百奥知产品实施及商务团队一行7人到达三生制药总部,三生制药临床运营团队约50人参会。百奥知针对eTMF和CTMS新版本,为客户进行了详尽的介绍和演示,用户在现场亲自进行了操作演练,通过实际体验,加深对系统的理解。经过3天的讲解和互动,三生制药所有参与人员均顺利掌握了新版本的功能特性,并通过了操作考核。不少用户对于新版本功能的改进也给予了高度赞赏。
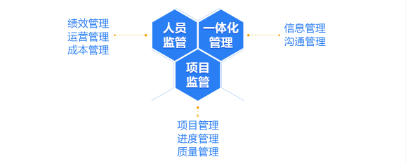
(绿色部分百奥知主导,蓝色部分三生制药主导)
三生制药eTMF、CTMS项目负责人对于本次培训会效果也表示满意,期待尽早将新版系统应用于临床研究工作中,提升整个临床研究的效率与质量。
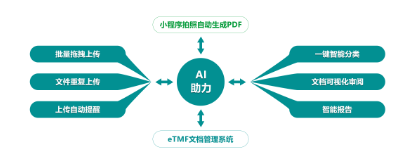
百奥知 eTMF
支持DIA文档管理的最新标准,让文档管理贯穿整个临床试验生命周期,帮助管理者实时监控项目文档,保证文档的完整、质量和时效。严格遵循ICH、NMPA发布的有关法律法规和指导原则,符合FDA 21CFR Part11有关电子记录与电子签名的要求。
百奥知 CTMS
通过对临床试验各个阶段的系统化管理,实现对试验项目的实时在线跟踪及监控。通过经费预算收支视图、进度甘特图、数据统计图等图形化方式,方便快捷掌握和管理多个项目的各个环节。系统符合NMPA、FDA、欧盟有关临床试验的质量管理的标准规范,符合FDA 21CFR Part11有关电子记录与电子签名的要求。
百奥知专注生命科技领域,提供覆盖临床前、临床、药物警戒和注册申报环节的全面产品与服务。集结临床数据解决方案(包含EDC-电子数据采集系统、RTSM-随机化与试验药物管理系统、CDTMS-临床数据全流程管理系统、MedCoding-医学编码系统等)、项目管理解决方案(包含项目管理系统CTMS、在线考核系统eTraning、临床试验读片与标本运送管理系统PDM等)、药物安全警戒解决方案(PV 系统)、文档管理解决方案(eTMF系统)四大解决方案10余款产品,实现临床研究流程的全覆盖,极大提升临床研究工作的便利和效率。
深耕医药研发全领域12年,凭借专业的技术力量与服务能力,累积为国内外1000多家申办方、CRO等客户的2300多个项目提供信息化解决方案,推动临床研究工作高效进行,赢得了众多客户的信任与认可。